Pubertad precoz y masa abdominal: reporte de un caso
Precocious Puberty and abdominal mass: a case report.
Caso Clínico
Dras. Zunana, Cecilia1, Peña, Teresa María2, Álvarez, Lucila 2, Califano, Paula Andrea3
Resumen
Introducción. La pubertad precoz en niñas, definida por la aparición de caracteres sexuales secundarios antes de los 8 años, puede ser de causa central o periférica. Esta última, menos frecuente, se puede asociar a secreción autónoma de esteroides sexuales. Las masas anexiales en edad pediátrica representan un desafío clínico debido a su heterogeneidad etiológica y a las posibles implicancias endocrinológicas y oncológicas. Caso clínico. Se reporta el caso de una niña de 8 años y 3 meses con sangrado genital y masa abdominal palpable. Entre los estudios complementarios se evidencian gonadotrofinas en rango prepuberal, niveles elevados de estradiol y edad ósea en el límite superior, compatibles con pubertad precoz periférica. Los estudios por imágenes demuestran una masa anexial voluminosa, de características sólido-quísticas. Con sospecha de neoplasia, se solicitan marcadores tumorales y se realiza abordaje quirúrgico mediante salpingo-ooforectomía unilateral con estadificación, confirmándose un tumor de células de la granulosa de tipo juvenil con rotura capsular. Dado el estadio, se indica quimioterapia adyuvante. De manera complementaria, y tras evaluación interdisciplinaria, se implementa preservación de la fertilidad mediante criopreservación de tejido ovárico del ovario contralateral macroscópicamente sano. La niña presenta evolución clínica favorable, con descenso sostenido de inhibina B, supresión de la producción estrogénica y regresión de los signos puberales. Los controles imagenológicos seriados no evidenciaron enfermedad residual ni recurrencia. Consideración final. El tumor de células de la granulosa juvenil, aunque infrecuente, debe considerarse ante pubertad precoz periférica asociada a masa anexial. El diagnóstico oportuno, la estadificación quirúrgica adecuada, la selección individualizada de terapias adyuvantes y la consideración temprana de estrategias de preservación de la fertilidad son determinantes para optimizar el pronóstico y la calidad de vida a largo plazo.
Palabras clave: Pubertad precoz; Neoplasias ováricas; DICER1; Preservación de la fertilidad. Tumor de células de la granulosa juvenil.
Abstract
Introduction. Precocious puberty in girls, defined as the development of secondary sexual characteristics before the age of 8 years, may be central or peripheral. The latter, less common form may be associated with autonomous secretion of sex steroids. Adnexal masses in the pediatric population represent a clinical challenge due to their etiologic heterogeneity and their potential endocrine and oncologic implications. Case report. We report the case of an 8-year- and 3-month-old girl who presented with genital bleeding and a palpable abdominal mass. Complementary studies showed gonadotropins within the prepubertal range, elevated estradiol levels, and bone age at the upper limit for chronological age, findings consistent with peripheral precocious puberty. Imaging studies demonstrated a large adnexal mass with solid-cystic characteristics. Given the suspicion of neoplasia, tumor markers were obtained and surgical management was performed with unilateral salpingo-oophorectomy and staging. Histopathological examination confirmed a juvenile granulosa cell tumor with capsular rupture. Based on staging, adjuvant chemotherapy was indicated. Additionally, following interdisciplinary evaluation, fertility preservation was undertaken through ovarian tissue cryopreservation of the contralateral macroscopically normal ovary. The patient showed favorable clinical evolution, with a sustained decline in inhibin B levels, suppression of estrogen production, and regression of pubertal signs. Serial imaging follow-up revealed no evidence of residual disease or recurrence. Final considerations. Although uncommon, juvenile granulosa cell tumor should be considered in cases of peripheral precocious puberty associated with an adnexal mass. Timely diagnosis, appropriate surgical staging, individualized selection of adjuvant therapy, and early consideration of fertility preservation strategies are critical to optimizing long-term prognosis and quality of life.
Keywords: Juvenile Granulosa Cell Tumor; Precocious Puberty; Ovarian Neoplasms; DICER1; Fertility Preservation
Introducción
La pubertad precoz se caracteriza por la aparición de signos de desarrollo puberal antes de los 8 años en niñas, con una prevalencia creciente en las últimas décadas. Este fenómeno puede clasificarse en pubertad precoz dependiente de gonadotrofinas (central) o independiente de gonadotrofinas (periférica), siendo la forma central la más común. La forma periférica suele relacionarse con producción autónoma de esteroides sexuales por tumores gonadales o suprarrenales.1 Como otras causales de pubertad precoz periférica isosexual en niñas por orden de frecuencia, se mencionan además los quistes ováricos autónomos, Síndrome de McCune-Albright, exposición exógena a estrógenos, hipotiroidismo primario severo.2 El cuadro clínico suele ser atípico ya que los signos puberales no presentan la secuencia de la pubertad normal, sino que en muchos casos se comienza con sangrado vaginal o bien simultáneamente con el inicio de la telarca.
Las masas anexiales en población pediátrica comprenden una amplia variedad de entidades, desde quistes autónomos hasta tumores neoplásicos, con una proporción menor de malignidad en comparación con adultos, pero con importantes implicancias diagnósticas y terapéuticas.1 Su abordaje debe incluir evaluación ecográfica como modalidad de elección inicial y, según el caso, métodos de imagen complementarios como resonancia magnética (RM).3 La presencia de una masa anexial en una niña con pubertad precoz exige la solicitud de marcadores tumorales y un abordaje multidisciplinario (diagnóstico por imágenes, ginecología, endocrinología, cirugía y oncología) para definir el tratamiento más apropiado.4 Además, el diagnóstico y el manejo médico/quirúrgico oportuno son clave para minimizar el impacto sobre el desarrollo fisiológico, la estatura final y la salud reproductiva futura de la niña.3
En este artículo se presenta un caso clínico de una niña de 8 años y 3 meses con pubertad precoz asociada a una masa anexial, con el objetivo de describir el abordaje diagnóstico y terapéutico, y discutir aspectos relevantes para la práctica en ginecología pediátrica.
Caso clínico
Se recibe derivación de una niña de 8 años y 3 meses para realizar valoración por pubertad precoz y hallazgo de masa abdominal. Había sido valorada el día previo por ginecólogos en su ciudad de origen por menarca precoz. En dicho contexto, se realizó una ecografía abdominal que informaba una gran imagen heterogénea, sólido-quística de aproximadamente 15 cm.
Al momento de la consulta, refiere dolor abdominal esporádico, de intensidad moderada, que cede de forma espontánea y en algunas oportunidades con analgésicos. No se asocia a síntomas gastrointestinales, sudoración nocturna, fiebre ni pérdida de peso. La madre relata que 3 meses previos a la menarca advirtió crecimiento mamario y de talla sin contar con registros. La menarca había sido a los 8 años y presenta ciclos regulares, de escasa cuantía y 4 días de duración. Como antecedentes familiares de relevancia, menciona la presencia de varios familiares de ambas ramas parentales con procesos oncológicos (mama, ovario, colon y leucemia).
Al examen físico, tiene buen estado general. La antropometría es: peso: 42 kg (Pc 95) Z +1.64, talla: 137 cm (Pc 50) Z -0.01, IMC: 22.38 kg/m2 (Pc 98) Z +2.02. La tiroides es no palpable, las mamas son Tanner 3 tróficas. El abdomen es blando y depresible con masa palpable en hipogastrio que alcanza 2 traveses de dedo sobre el ombligo. La misma resulta dura, indolora, de aproximadamente 15 cm. El vello púbico es Tanner 2, los genitales tróficos y conservados.
Se realizó nueva ecografía en el hospital que informa masa en topografía centro abdominal, de aproximadamente 14 x 9.7 x 13.3 cm (ver Imagen 1). El útero mide 5,5 cm en su diámetro máximo. No se logran identificar ovarios derecho o izquierdo. Se solicita radiografía de mano izquierda para valorar edad ósea la cual, según el atlas de carpograma de Oxford 2011, evidencia edad ósea de 10 años para cronológica de 8 y 3 meses.
Con sospecha de neoplasia, se solicita laboratorio con parámetros de lisis, hormonas y marcadores tumorales. Se obtienen valores elevados de inhibina B mayor a 3000 pg/ml (valor normal 9.5- 120 pg/ml), CA-125: 239 U/mL (valor normal 4.7-36 U/mL) y LDH 500 UI/L (valor normal 0-306). Resto de marcadores (AFP, β-hCG, CEA, CA 19-9) dentro de límites normales. Las gonadotrofinas resultan LH y FSH 0.06 MIU/ml (ambas en rango prepuberal) con estradiol de 103 pg/dl.
Se solicita RM de pelvis con contraste que evidencia formación tumoral abdomino-pelviana central en íntimo contacto con el peritoneo sin claro plano de clivaje con el mismo. La misma presenta bordes bien definidos de intensidad heterogénea multiquística con tabiques y realce heterogéneo con contraste. Se identifican áreas de restricción en difusión. Mide: 14.4 x 7.4 x 14,2 cm (ver imagen 2). La imagen impresiona en relación al anexo derecho. Se evidencia dilatación urétero-pielocalicial derecho.
Luego de la evaluación integral e interdisciplinaria, se procede a realizar una laparoscopía exploradora. Los hallazgos intraoperatorios incluyen: tumor anexial derecho de 20 cm con evidencia de ruptura capsular previa (presencia de adherencias firmes de epiplón a la superficie tumoral), útero y anexo contralateral de aspecto normal y un implante peritoneal sospechoso en cara anterior periumbilical. Se toma biopsia de este último y de líquido peritoneal. Se realiza salpingo-ooforectomía derecha unilateral y omentectomía por características de los hallazgos intraquirúrgicos (ver imagen 3). La estadificación quirúrgica según criterios FIGO (2021) es Estadio IC2 (debido a la rotura intraabdominal previa a la cirugía).
El estudio histopatológico confirma un Tumor de Células de la Granulosa de tipo Juvenil (TCGJ). Se observan cambios necrótico-isquémicos compatibles con un evento de torsión anexial previa. El epiplón presentó hiperplasia mesotelial reactiva, sin evidencia de infiltración neoplásica. La citología del líquido peritoneal resulta negativa. La Clasificación final es pT1c2 N0 M0. Tras la confirmación histopatológica del diagnóstico, el servicio de Oncología Médica prescribe un régimen de quimioterapia adyuvante basado en el esquema VIP (Etopósido, Ifosfamida y Cisplatino). Previo al mismo, se realizan estudios basales (tomografía computada de tórax, audiometría y pruebas de función pulmonar). Se procede al asesoramiento conjunto entre equipo oncología y cirugía general para realizar preservación de la fertilidad mediante criopreservación del tejido ovárico del ovario macroscópicamente sano contralateral. Ante el interés de ambos padres, se contacta a los mismos con un equipo de centro de fertilidad privado donde se realiza asesoría técnica exhaustiva sobre el procedimiento y la criopreservación que queda a cargo de dicho centro. Allí se detalla la relación costo-beneficio, los riesgos inherentes y el alcance clínico de la técnica. En el mismo acto que la colocación de catéter, se realiza laparoscópica con sección de 1 cm de corteza ovárica y cuidadosa hemostasia.
Debido a la presencia de antecedentes familiares de cáncer y la histología del tumor, se solicita la secuenciación del gen DICER1, por su asociación conocida con tumores de cordones sexuales en pediatría.
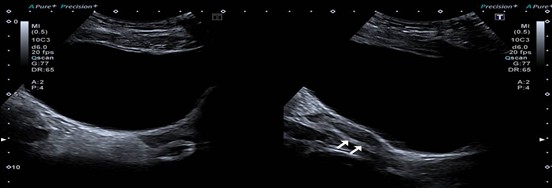
Se realiza RM de control tras el segundo y cuarto ciclo de quimioterapia, sin evidencia de enfermedad residual ni recidiva. La ecografía postquirúrgica presenta útero más pequeño con diámetro longitudinal de 35 mm. (Ver imagen 4). Asimismo, se realizan dosajes seriados de inhibina B con resultados de 33, 20, 10, 12 pg/ml luego de cada ciclo de quimioterapia y estradiol, que resultan no dosables en todas las muestras. La niña continúa en seguimiento clínico-radiológico y monitorización de marcadores tumorales (Inhibina/Estradiol) con evolución favorable. En el examen físico de mamas y genitales, se evidencia menor trofismo que previo a la cirugía. No presentó más deprivaciones.
Discusión
Frente al diagnóstico de pubertad precoz, resulta fundamental diferenciar si se trata de un proceso central (dependiente de gonadotrofinas) o periférico (independiente de las mismas). En el caso presentado, tanto FSH como LH se encontraban en rangos prepuberales, con estradiol elevado y una edad ósea en el límite superior a 2 desvíos estándar. Estos parámetros permitieron establecer el origen periférico del cuadro, hallazgos concordantes con lo reportado en series pediátricas de tumores productores de estrógenos. 5, 6 En la población pediátrica, toda masa ovárica sólida debe considerarse potencialmente maligna hasta demostrarse lo contrario mediante estudio histopatológico.1 Sin embargo, el grado de sospecha debe ser el resultado de una cuidadosa valoración de la clínica, junto con los estudios por imágenes que contemple las características de las mismas (patrón sólido, heterogénea, tamaño, etc.) y los marcadores tumorales.
Las masas ováricas en la infancia y la adolescencia presentan un amplio espectro etiológico; sin embargo, se estima que entre el 10 y el 20 % son de naturaleza maligna. Dentro de este grupo, los tumores de los cordones sexuales y del estroma representan aproximadamente el 5 % de las neoplasias ováricas pediátricas, siendo el tumor de células de la granulosa de tipo juvenil (TCGJ) una entidad infrecuente (menos de 0.5% de todos los tumores incluidos en el ítem varios e inespecíficos del último Registro Oncopediátrico Hospitalario Argentino). Sin embargo, es relevante por su comportamiento endocrino y sus precoces manifestaciones clínicas.7,8
El TCGJ se diferencia claramente de su variante adulta, tanto desde el punto de vista clínico como histopatológico. En la infancia 2/3 de las niñas con estos tumores cursan con pubertad precoz isosexual secundaria a la capacidad de secreción autónoma de estrógenos.6 En el caso presentado, éste fue el síntoma cardinal, lo que coincide con lo descrito en la literatura.
Desde el punto de vista imagenológico, la RM constituye una herramienta clave para la caracterización de las masas ováricas. El patrón multiquístico con componente hemorrágico, descrito como aspecto “en esponja”, observado en este caso, es un hallazgo sugestivo de TCGJ y puede contribuir a su diferenciación respecto de los tumores de células germinales, más frecuentes en este grupo etario.7
Los marcadores tumorales desempeñan un papel complementario en la evaluación diagnóstica y el seguimiento. Si bien la elevación de CA-125 y LDH es inespecífica y se asocia principalmente al volumen tumoral, la inhibina B (en el caso mayor a 3000UI/l) se considera el marcador más sensible y específico para los tumores de células de la granulosa, tanto en el diagnóstico inicial como en la detección precoz de recurrencias.6 El perfil de estos marcadores refuerza la necesidad de una interpretación integrada de los hallazgos clínicos, bioquímicos e imagenológicos antes y después del tratamiento.
El tratamiento del TCGJ es fundamentalmente quirúrgico y, en pacientes pediátricas, debe priorizarse un enfoque conservador con preservación de la fertilidad siempre que sea posible. La estadificación de estos tumores en la población pediátrica se basa en el sistema FIGO, con adaptaciones propuestas por el Grupo de Oncología Infantil- Children’s Oncology Group, que identifican un mayor riesgo de recurrencia en estadios avanzados y en presencia de lavado peritoneal positivo. Estos hallazgos subrayan la importancia de una técnica quirúrgica cuidadosa orientada a evitar la rotura capsular, dado su impacto en el pronóstico a largo plazo. 5,6
En el presente caso, la rotura tumoral accidental determinó un estadio FIGO IC2, lo que condicionó la indicación de quimioterapia adyuvante, en concordancia con las recomendaciones actuales para reducir el riesgo de recaída.9
En relación la preservación de la fertilidad, Academia Estadounidense de Pediatría y la Sociedad Estadounidense de Medicina Reproductiva coinciden en que la criopreservación de tejido ovárico debe ofrecerse a niñas con alto riesgo de insuficiencia ovárica prematura, en centros con experiencia y bajo protocolos de investigación o programas clínicos establecidos. Sin embargo, la decisión debe ser individualizada, considerando el mencionado riesgo de insuficiencia ovárica prematura, el estadio y la posibilidad de cirugía conservadora. Es fundamental realizar una evaluación histológica del tejido para descartar la presencia de células malignas, ya que existe el riesgo teórico de reintroducción tumoral frente a un eventual autotrasplante, especialmente en tumores ováricos. En estos últimos, la recolección de tejido debe realizarse del ovario macroscópicamente sano. Según se describe en la literatura, la eficacia de la criopreservación en niñas prepuberales es todavía considerada experimental por varios autores. Se han reportado casos de embarazos tras autotrasplante en pacientes pediátricas o cultivo in-vitro de ovocitos de dicho tejido. Resulta entonces esencial informar a la familia sobre las limitaciones y el carácter experimental del procedimiento, así como sobre los riesgos quirúrgicos y la posibilidad de insuficiencia ovárica en el futuro. 1, 10
Finalmente, en los últimos años ha cobrado relevancia la asociación entre el TCGJ y mutaciones en el gen DICER1. En pacientes con antecedentes familiares oncológicos significativos, como en el caso presentado, el estudio genético resulta fundamental no solo para el asesoramiento familiar, sino también para el cribado de otras neoplasias asociadas, como el blastoma pleuropulmonar y el bocio multinodular, permitiendo una estrategia de seguimiento integral.11 En el caso presentado, dicho estudio se encuentra aún pendiente al momento de la publicación.12
Consideraciones finales
El tumor de células de la granulosa de tipo juvenil constituye una causa infrecuente pero relevante de masas ováricas en la infancia, especialmente cuando se asocia a pubertad precoz periférica isosexual. Su diagnóstico requiere un alto índice de sospecha clínica y una evaluación integral que combine hallazgos de laboratorio, imagenológicos y anatomopatológicos. El abordaje quirúrgico conservador es el pilar del tratamiento; no obstante, la rotura capsular intraoperatoria representa un factor que condiciona la necesidad de tratamiento adyuvante y un seguimiento estrecho. Finalmente, el reconocimiento de la asociación con mutaciones en DICER1 resalta la importancia del asesoramiento genético y de una estrategia de vigilancia integral en pacientes con antecedentes familiares oncológicos.
Bibliografía
- Emans, S. Jean, Marc R. Laufer, and Donald P. Goldstein. Pediatric and Adolescent Gynecology. 7th ed., Wolters Kluwer, 2020, pp. 351–361.
- Argente, Jesús, et al. “Molecular Basis of Normal and Pathological Puberty: From Basic Mechanisms to Clinical Implications.” The Lancet Diabetes & Endocrinology, vol. 11, no. 3, 2023, pp. 203–216. Elsevier, doi:10.1016/S2213-8587(22)00339-4
- Bourgioti, Charis et al. “Imaging Evaluation of Ovarian Masses in a Pediatric Population: A Comprehensive Overview.” Cancers 17,14 2316. 11 Jul. 2025, doi:10.3390/cancers17142316
- Mentessidou, Anastasia, and Petros Mirilas. “Surgical disorders in pediatric and adolescent gynecology: Adnexal abnormalities.” International journal of gynaecology and obstetrics: the official organ of the International Federation of Gynaecology and Obstetrics 161,3 (2023): 702-710. doi:10.1002/ijgo.14574
- Schultz, Kris Ann P et al. “Management of ovarian and testicular sex cord-stromal tumors in children and adolescents.” Journal of pediatric hematology/oncology 34 Suppl 2 (2012): S55-63. doi:10.1097/MPH.0b013e31824e3867)
- “Juvenile granulosa cell tumor.” eMedicine Medscape, section on Sex Cord Stromal Ovary Tumor Pathology, Medscape, updated 2025, emedicine.medscape.com/article/1627984-overview
- Young, Robert H. “Ovarian sex cord-stromal tumours and their mimics.” Pathology 50,1 (2018): 5-15. doi:10.1016/j.pathol.2017.09.007
- Moreno, Florencia, and María Agustina Chaplin. Registro Oncopediátrico Hospitalario Argentino. 7a ed., Instituto Nacional del Cáncer, 2025. https://www.argentina.gob.ar/sites/default/files/2024/04/manual_registro_oncopediatrico_hospitalario_argentino_1642025.pdf?utm_source=chatgpt.com)
- Renz, Malte et al. “Cancer of the ovary, fallopian tube, and peritoneum: 2025 update.” International journal of gynaecology and obstetrics: the official organ of the International Federation of Gynaecology and Obstetrics vol. 171 Suppl 1, Suppl 1 (2025): 6-35. doi:10.1002/ijgo.70282
- Mulder, Renée L et al. “Fertility preservation for female patients with childhood, adolescent, and young adult cancer: recommendations from the PanCareLIFE Consortium and the International Late Effects of Childhood Cancer Guideline Harmonization Group.” The Lancet. Oncology vol. 22,2 (2021): e45-e56. doi:10.1016/S1470-2045(20)30594-5
- Schultz, Kris Ann P et al. “DICER1-related Sertoli-Leydig cell tumor and gynandroblastoma: Clinical and genetic findings from the International Ovarian and Testicular Stromal Tumor Registry.” Gynecologic oncology 147,3 (2017): 521-527. doi:10.1016/j.ygyno.2017.09.034).
- Roumpou, Afroditi et al. “A Novel Pathogenic Variant of DICER1 Gene in a Young Greek Patient with 2 Different Sex-Cord Ovarian Tumors and Multinodular Goiter.” International journal of molecular sciences 26,5 1990. 25 Feb. 2025, doi:10.3390/ijms26051990
Figura 1. Ecografía abdominal del ingreso. Se visualiza voluminosa masa en topografía centro abdominal, sólido-quística a predominio sólido de 14 x 9.7 x 1.3 cm.
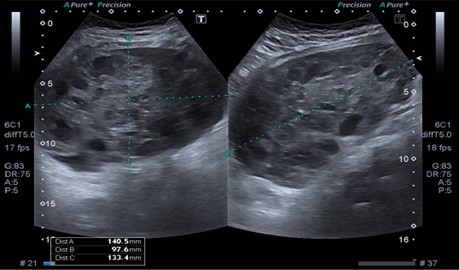
Imagen 2. Resonancia magnética. Cortes coronal y sagital en t2. Se identifica formación tumoral abdominopelviana central en íntimo contacto con el peritoneo sin claro plano de clivaje con el mismo. La misma es ovoidea de bordes bien definidos de intensidad heterogénea multiquística con tabiques y realce heterogéneo con contraste. Mide: 14.4 x 7.4 x 14,2 cm que podría corresponder a tumor de estirpe moderado a agresivo con componentes seroso-mixto.
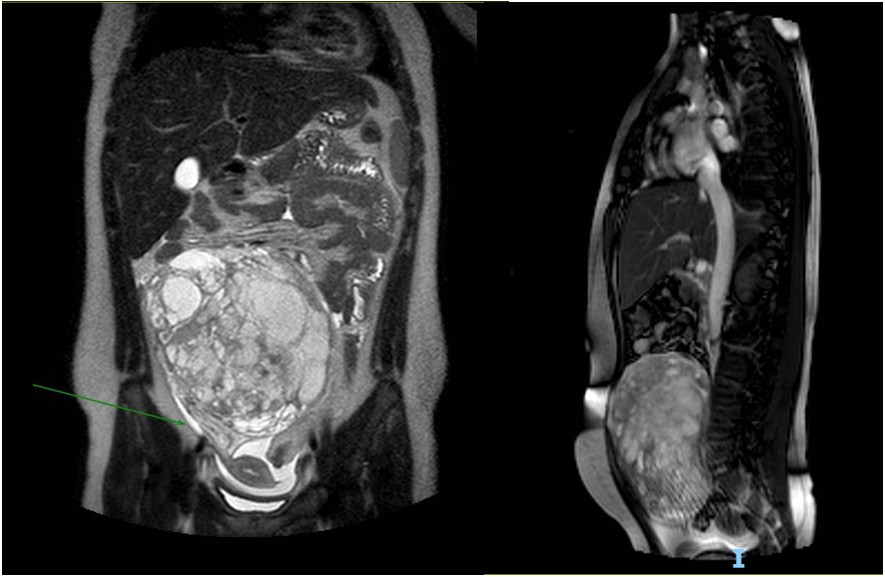
Imagen 3. Fotografía de pieza quirúrgica. Voluminosa formación polilobulada con cápsula rota.
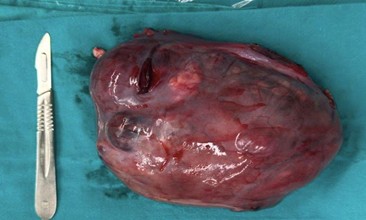
Imagen 4. Ecografía ginecológica de control post operatoria. Útero Tubular en línea media. Mide 3.4x1x0.9 cm, endometrio lineal, Ovario Derecho: ausente acorde a antecedentes. Ovario Izquierdo: En FII de ecoestructura conservada. Mide 1.1x1x0.6 cm Volumen 0.3 cc.
- Médica ginecólogas certificadas en Ginecología Infanto Juvenil. Médica de planta en la Unidad de Ginecología Infanto Juvenil.
- Médica cirujana infantil. Médica de planta del servicio de Cirugía General.
- Médica ginecóloga certificada en Ginecología Infanto Juvenil. Coordinadora de la Unidad de Ginecología Infanto Juvenil
