Programa de preservación de la fertilidad en pacientes pediátricos y adolescentes.
Fertility preservation program for pediatric and adolescents’ patients.
Trabajo Original
Lucila Othatz1, Ines Sueiras2, Paula Violo3, Pablo Lobos4, Patricia Streitenberger5, Romina Pesce6, Laura Cesarato7, Mariela Orti8, Juan Moldes, Maria Ormaechea9
Resumen
Objetivo: El objetivo del trabajo es la descripción de una población de pacientes que por trastornos oncológicos fue sometida a tratamientos de preservación de la fertilidad. Numerosas razones justifican la formación de un programa de preservación de fertilidad en pediatría. Las situaciones y patologías que convocan a pensar en la preservación de la fertilidad son varias: patología oncológica, autoinmune, genética, desórdenes de la diferenciación sexual (DSD), patología benigna y pacientes transgénero.
En la actualidad, la primera causa es la oncofertilidad pediátrica. En este caso son pacientes que se van a someter a algún tipo de tratamiento gonadotóxico por patología oncológica. Hoy en día, gracias a las nuevas alternativas terapéuticas, la expectativa de vida post quimioterapia por cáncer infantil ha aumentado en forma significativa en la última década, por lo que la fertilidad se ha convertido en una de las principales preocupaciones.
Materiales y métodos: Se presenta la primera serie de cinco casos de entre 16 y 17 años, abordados en el Hospital Italiano de Buenos Aires, por el equipo de preservación de la fertilidad, durante el período de febrero a junio de 2021. Se evaluó en forma interdisciplinaria a cada paciente. Se decidió ofrecer la mejor estrategia de preservación de fertilidad, adecuada según la posibilidad que implica, el tiempo disponible para realizarlo, la edad, el grado y compromiso de la enfermedad de base y su pronóstico.
En el período analizado, se realizó tratamiento de criopreservación de la fertilidad a 5 pacientes. La edad media de los pacientes fue de 16,8 años (Rango de edad: 16 a 17 años).
Resultados: Las patologías de base fueron: sarcoma de Ewing en una paciente, osteosarcoma de fémur en tres pacientes y un disgerminoma de ovario en otra. Las cinco pacientes fueron evaluadas y asesoradas por el equipo multidisciplinario comprendido por oncología, endocrinología, cirugía pediátrica, urología pediátrica, reproducción y ginecología pediátrica/adolescente, para definir la mejor estrategia. En 2 pacientes se decidió la estimulación ovárica con aspiración folicular y posterior vitrificación de ovocitos. En estos casos se obtuvieron entre 15 a 38 ovocitos de buena calidad. En las 3 pacientes restantes se decidió la preservación de tejido ovárico, obtenido por vía laparoscópica y siendo la muestra suficiente. En todos los casos las pacientes comenzaron con su quimioterapia según los tiempos indicados, sin verse demorado su tratamiento. Conclusión: Es fundamental poder contar con un programa de preservación de fertilidad interdisciplinario para lograr una derivación precoz y adecuar la mejor estrategia a realizar. La derivación tardía al especialista, es la causa más frecuente de retraso en el tratamiento. Es necesario seguir incorporando pacientes con otras patologías que requieran asesoramiento y evaluación de la preservación de la fertilidad a futuro.
Palabras clave: fertilidad, preservación fertilidad, pacientes oncológicos, pediatría
Abstract
Objective: The objective of this work is to describe a population of patients with recent diagnosis of cancer, that was presented on a fertility preservation program.
Many reasons justify the promotion of a fertility preservation program on pediatric patients. Pathologies in which fertility preservation should be considered include oncologic, autoimmune and genetic diseases, disorder of sexual differentiation (DSD), recurrent benign pathology and transgender patients.
Currently, the leading cause is pediatric oncofertility, which includes patients who will undergo some type of gonadotoxic treatment for oncological pathology. With the new therapeutic alternatives, life expectancy after chemotherapy for childhood cancer has increased significantly in the last decade, so fertility preservation has become one of the main concerns.
Patients and methods: This study presents the first case series of five patients between 16 and 17 years old, informed and treated at Italian Hospital of Buenos Aires by the fertility preservation team, between February and June 2021. Each patient was interdisciplinary evaluated. We offered the best fertility strategy, appropriate according to the possibility involved, the time available to carry it out, the age, the extent and progression of the underlying disease and its prognosis. We treated five patients for fertility preservation. Mean age was 16.8 years old.
Results: The oncologic pathology diagnoses were Ewing Sarcoma in one patient, femur osteosarcoma in three patients, and one dysgerminoma. All the patients were evaluated and advised by the interdisciplinary team (which includes oncologist, endocrinologist, pediatric surgeon, pediatric urology, pediatric and adolescent gynecologist) to perform the best strategy. Two patients were offered oocyte stimulation, and 15-38 oocytes of good quality were obtained. A sufficient portion of ovary tissue was obtained by laparoscopy in the last three patients.
The patients began their chemotherapy according to the times indicated, without delaying their treatment.
Conclusion: It's necessary to have an interdisciplinary fertility preservation program for an early referral and offer the best strategy for preservation. The greatest loss of opportunity to carry out an effective preservation treatment is the lack or delay in referral.
It is necessary to incorporate patients with other pathologies that require advice and evaluation of the preservation of fertility in the future.
Key words: fertility, fertility preservation, oncologic patients, pediatrics
Introducción
La mayoría de los niños con cáncer sobreviven y ese incremento en la supervivencia ha puesto de manifiesto secuelas directamente relacionadas con la agresividad del tratamiento aplicado y el tipo de neoplasia tratada, así como un incremento del riesgo de fallecimiento por otras causas. En estos momentos, ya no es suficiente el concepto de “curar a cualquier costo”. El objetivo es ofrecer una recuperación completa, con una buena calidad de vida y una reintegración plena en la sociedad. Por este motivo, el desarrollo de protocolos y grupos de trabajo interdisciplinario conformados por profesionales de diferentes subespecialidades como oncohematología pediátrica, cirugía pediátrica, ginecología infanto juvenil, endocrinología, pediatría, salud mental y medicina reproductiva se han multiplicado enormemente en los últimos años.
La población principal dentro del programa de preservación de la fertilidad incluye pacientes tanto premenárquicas como postmenárquicas, que van a recibir algún tipo de tratamiento gonadotóxico y/o que se ven afectadas por alguna condición genética que reduce su periodo reproductivo. Otras posibles causas descriptas son las pacientes transgénero, la patología ovárica benigna recurrente, la patología autoinmune y las múltiples causas genéticas.
Dado que la expectativa de vida en pacientes menores de 15 años post tratamiento quimioterápico por cáncer infantil ha aumentado en los últimos tiempos, la fertilidad se ha convertido en una de las principales preocupaciones tanto de los profesionales de la salud como del paciente y su entorno familiar. (1), (2)
En beneficio de las nuevas alternativas terapéuticas, ha aumentado la expectativa de vida en pacientes que se someten a tratamiento quimioterápico por cáncer infantil en forma significativa en la última década, hasta alcanzar un 80%. Esto ubica la fertilidad dentro de una de las principales preocupaciones. El mayor conocimiento sobre la importancia de la preservación de la fertilidad para pacientes pediátricos y adolescentes con cáncer y mejoras en las técnicas de reproducción asistida han aumentado la probabilidad de que el cumplimiento de las metas de planificación familiar para los sobrevivientes de cáncer haya mejorado y continúe mejorando con el tiempo. (3)
Los trastornos endocrinos, incluida la disfunción y la insuficiencia ovárica prematura, son las enfermedades crónicas más frecuentes en los sobrevivientes de cáncer infantil y pueden aparecer años después del tratamiento. La insuficiencia ovárica aguda se define por una amenorrea primaria o secundaria después de un tratamiento de alto riesgo gonadotóxico.(1)
El modelo de trabajo de esta sección implica necesariamente ser interdisciplinario. El médico especialista en fertilidad pediátrica tendrá́ que coordinar el tratamiento ideal para el paciente con distintos especialistas. Es fundamental el trabajo en equipo para lograr una derivación precoz y lograr adecuar la mejor estrategia para la preservación.
Una de las estrategias para lograr una mayor divulgación tanto intra como extrahospitalaria es la realización de conferencias o presentaciones para las distintas especialidades clínicas (pediatría, hematología pediátrica, reumatología pediátrica, endocrinología pediátrica etc.). La mayor pérdida de oportunidades de realizar un tratamiento efectivo de preservación es la derivación tardía, o la falta de derivación por el médico tratante.
Material y método
Se presenta la primera serie de cinco casos de entre 17 y 18 años, asesorados y tratados en el Hospital Italiano de Buenos Aires por el equipo de preservación de la fertilidad en el período de febrero a junio del 2021. Se realizó una evaluación completa multidisciplinaria de cada paciente.
Los estudios iniciales de las pacientes incluyeron: historia clínica completa, momento del ciclo ovulatorio, evaluación de reserva ovárica con la medición de la hormona antimulleriana (AMH) y recuento de folículos antrales. Esto último es algo posible de realizar únicamente en pacientes postpuberales (en fase folicular temprana), y no así en niñas prepuberales.
En base a la historia clínica y estudios de cada paciente, se ofreció la mejor estrategia de fertilidad, adecuada según la posibilidad que implica, el tiempo que se dispone para realizar un tratamiento, la edad, el grado y compromiso de la enfermedad y su pronóstico
Resultados
En el período analizado, se realizaron tratamientos de criopreservación de la fertilidad a 5 pacientes. Edad media 16,8 años.
Las patologías de base diagnosticadas fueron: sarcoma de Ewing (n=1), osteosarcoma de fémur (n=3) y disgerminoma (n=1).
Las 5 pacientes fueron evaluadas y asesoradas por el equipo interdisciplinario (oncología, endocrinología, cirugía pediátrica, urología pediátrica, ginecología infantojuvenil) para la definir la mejor estrategia.
Luego de la evaluación, en 2 pacientes se realizó estimulación de ovocitos, siguiendo el protocolo de estimulación. Se obtuvieron en todos los casos un promedio entre 15 a 38 ovocitos de buena calidad. En el grupo restante de las 3 pacientes que no realizaron vitrificación de ovocitos, se procedió a realizar la preservación de tejido ovárico con obtención por vía laparoscópica de material suficiente.
El alta hospitalaria luego del procedimiento fue a las 24 hs. en todos los casos y sin complicaciones quirúrgicas. Todas las pacientes pudieron comenzar con su quimioterapia a tiempo. (Cuadro 1)
|
Paciente |
Edad (años) |
Diagnóstico |
Tratamiento Fertilidad |
|
I |
17 |
Disgerminoma de ovario |
Criopreservación tejido ovárico |
|
II |
17 |
Sarcoma Ewing |
Criopreservación de tejido ovárico |
|
III |
17 |
Osteosarcoma de Fémur |
Estimulación y aspiración de ovocitos |
|
IV |
16 |
Osteosarcoma de fémur |
Criopreservación de tejido ovárico |
|
V |
17 |
Osteosarcoma de Fémur |
Estimulación y aspiración ovocitos |
Cuadro 1: Edades, patología y tratamiento de los 5 casos evaluados
Discusión
El tipo de cáncer, la edad, el desarrollo puberal, la gravedad de la enfermedad en el momento del diagnóstico y el tipo de tratamiento influyen en la toma de decisiones relacionadas con la preservación de la fertilidad (2,3). Los pacientes con mayor riesgo de toxicidad gonadal incluyen aquellos que reciben agentes alquilantes en dosis altas y/o la radiación pélvica que conduce al agotamiento de la reserva ovárica. (4)
La radiación dirigida al cerebro puede interferir con el eje hipotalámico-pituitario-gonadal y afectar la capacidad de los ovarios para funcionar correctamente.
Es importante identificar alto riesgo de esterilidad, sobre todo en aquellas pacientes que han recibido radioterapia previa o trasplantes de médula ósea. La dosis para producir insuficiencia ovárica precoz en una mujer de 30 años es de 16Gy. Hay que considerar que dosis de 2Gy producen una depleción folicular de hasta el 50% de la reserva ovárica.
Las terapias dirigidas contra el cáncer que implican la resección quirúrgica de las estructuras reproductivas tienen claras implicaciones para la fertilidad posterior.
Las situaciones y patologías que convocan a pensar en la preservación de la fertilidad son varias: patología oncológica, autoinmune, genética, desórdenes de la diferenciación sexual (DSD), patología benigna y pacientes transgénero.
Ante la identificación de un paciente con riesgo de perder su potencial reproductivo, el medio a cargo debe solicitar la evaluación de un especialista en oncofertilidad pediátrica. Su función será́ evaluar al paciente a la brevedad. Se debe tomar la interconsulta de oncofertilidad con carácter de urgencia. Idealmente la paciente debe ser asesorada en el mismo día que se recibe la derivación. El especialista en fertilidad debe evaluar el status del paciente, el tiempo disponible para instaurar una estrategia de preservación y la terapia gonadotóxica. Con estas variables se diseña un plan de acción que será adecuado sin interferir en el tratamiento primario de la enfermedad de base y se realizará el asesoramiento oportuno. (Fig. 1) (5)
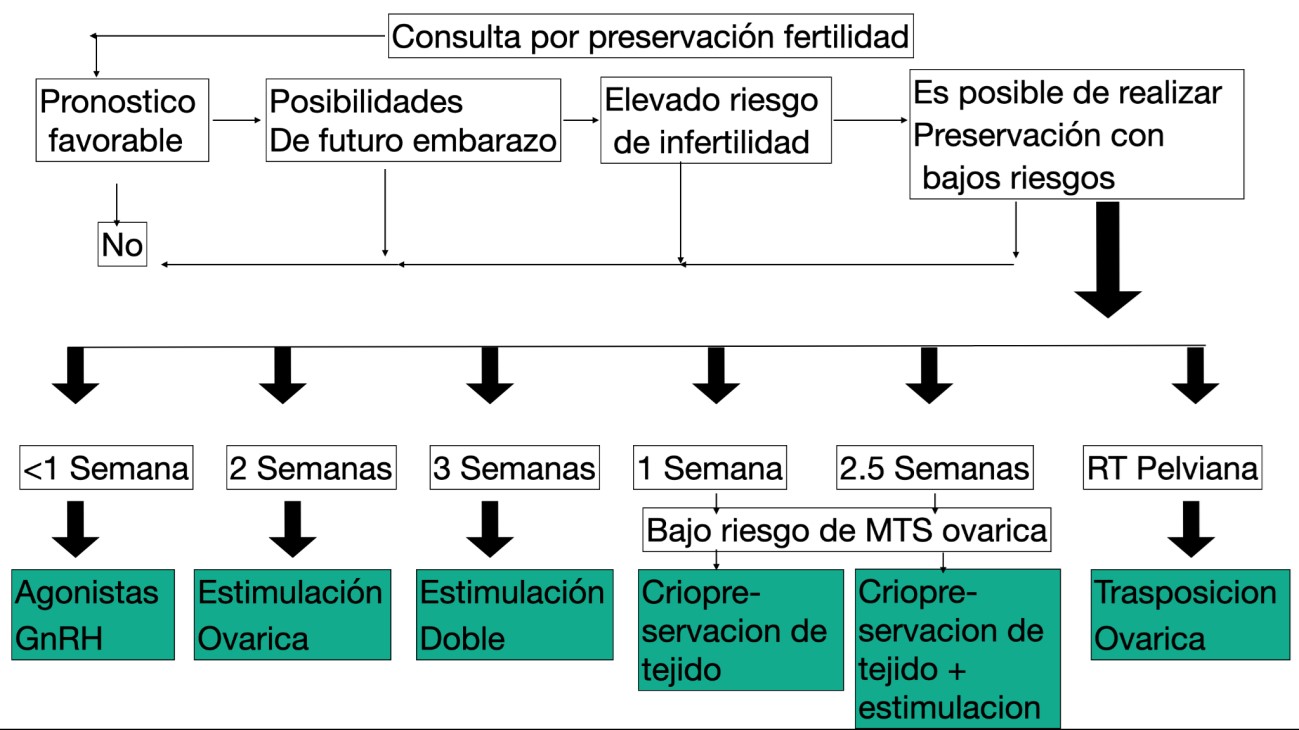
Fig. 1: Gráfico adaptado y extraído de “Practical recommendations for fertility preservation in women by the FertiPROTEKT network”. Part I: Indications for fertility preservation A. N. Schüring1 · T. Fehm.2017
Los estudios iniciales de la paciente deberían incluir: historia clínica completa, diferenciando en primera instancia la paciente prepuberal de la pospuberal. Evaluar el momento del ciclo ovulatorio, midiendo la reserva ovárica con la hormona antimulleriana y recuento de folículos antrales en los casos que sea factible. Una vez realizada la evaluación completa y habiendo discutido con el equipo de médicos tratantes se deberá realizar el asesoramiento oportuno y adecuar el tratamiento más conveniente. (6)
Dentro de las diferentes técnicas para preservación de fertilidad contamos con:
Criopreservación de ovocitos:
Consiste en provocar la estimulación ovárica para lograr desarrollar el mayor número de folículos posibles. Se realiza mediante la aplicación de gonadotrofinas. A continuación, se obtienen los ovocitos mediante una punción transvaginal. Idealmente se comienza al principio del ciclo menstrual, pero se ha demostrado que puede realizarse durante cualquier periodo de este. Incluso, puede realizarse doble estimulación o estimulación luego de recolección de tejido ovárico. El número de ovocitos y el porcentaje de éxito (recién nacido vivo) se correlaciona con la edad y la reserva ovárica de la paciente. (2)
Para realizar la criopreservación de ovocitos en pacientes post menárquicas, se debe promover la toma de decisión compartida. Documentar la decisión, evaluando los riesgos y beneficios, daños y costos, la logística y el mantenimiento. Hay que considerar el estado general, riesgos asociados a la práctica, la posibilidad de retraso en inicio de terapia por falta de madurez emocional, y adecuar las necesidades según creencia religiosas y culturales.
En aquellas pacientes con riesgo de recurrencia de tumores Borderline de ovario, es recomendable de realizar. No así, en aquellas con un ovario, sin riesgo de enfermedad recidivante o recurrente, dado que el riesgo supera el beneficio del procedimiento.
Criopreservación de tejido ovárico:
Se recomienda reservar está técnica para niñas prepúberes (casi como opción exclusiva) o pospúberes sin otros métodos posibles, que no tienen tiempo para la estimulación ovárica. (4)(7)
Los riesgos son reducidos y en determinadas pacientes se realiza en el mismo acto quirúrgico con la resección de la masa tumoral. Existen casos reportados de mujeres que criopreservaron tejido en etapa prepuberal y lograron restablecer la función hormonal y reproductiva luego del retrasplante de tejido. (8)
Desde hace 10 años los criterios planteados por el equipo de Wallace en Edimburgo han sentado las bases de los programas de preservación de fertilidad para las indicaciones de preservación de tejido ovárico, que incluyen a pacientes menores y globalmente son aceptados.
Las indicaciones de esta técnica deben cumplir los Criterios de Edimburgo 4: (9)
Cuadro 2. Criterios de Edimburgo 4: (9)
|
Pacientes <35 años con buena reserva ovárica. |
|
Sin antecedentes de tratamiento gonadotóxico previo. |
|
Sobrevida real >5 años. |
|
Riesgo esterilizante >50%. |
|
En niñas o prepúberes contar con autorización de los padres o representante legal y firmar consentimiento informado. |
|
Serologías negativas. |
|
Mujer sin hijos. |
Una consideración en este punto son las pacientes que presentan patología de estirpe ovárica, ya que, al tener mayor riesgo de contaminación en el tejido preservado, la gran mayoría no se realiza el trasplante en el futuro, por riesgo a implantación de células neoplásicas. Por lo cual se realiza estimulación del tejido, y luego tratamiento de fertilidad asistida. (7)
Agonista GnRH:
Su indicación estaría en su potencial efecto protector. La hipótesis de menor afectación del ovario ante drogas gonadotóxicas, por acción inhibitoria y de “down regulation” de los agonistas del GnRH. Existen otros mecanismos protectores que no están claros. Por eso, esta opción sigue siendo de rango “experimental” y generalmente se reserva para terapia complementaria o como terapia única, en aquellas pacientes que no pueden acceder a otra opción de preservación.
Transposición ovárica:
Esta opción se debe considerar cuando la paciente va a recibir radioterapia en la zona pélvica. Además de los riesgos y beneficios, se deberían discutir alternativas como criopreservación de ovocitos y/o tejido ovárico. (Figura 2) (7,10)
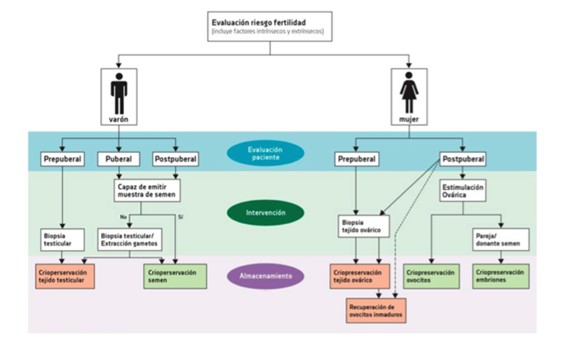
Fig.2 Algoritmo. Extraído y adaptado de: Anderson RA. Cancer treatment and gonadal function: experimental and established strategies for fertility preservation in children and young adults (2015) (4)
Todos los casos de asesoramiento de preservación de fertilidad deberían ser registrados de forma activa. (11) El mismo servirá ́ para realizar seguimiento con asesoramiento posterior al tratamiento oncológico. A su vez permitirá ́ realizar recopilación de datos para realizar trabajos de investigación.
Conclusión:
El aumento de la supervivencia en pacientes oncológicos y el avance en las técnicas de reproducción asistida hacen que hoy en día los profesionales debamos considerar el tratamiento de preservación de fertilidad en una población cada vez mayor. Es responsabilidad de los profesionales ser conscientes de esta posibilidad de tratamiento para realizar así una derivación oportuna.
Es fundamental contar con un programa y equipo multidisciplinario de preservación de fertilidad, para acompañar al paciente y su familia desde el diagnóstico, lograr una derivación precoz y adecuar la mejor estrategia de preservación.
El principal factor en la perdida de oportunidad para realizar un tratamiento efectivo de preservación es no derivar o derivar de manera tardía al paciente.
Por ende, es necesario seguir incorporando pacientes con otras patologías, que requieran asesoramiento y evaluación de la preservación de la fertilidad a futuro.
Bibliografía
- Wallace WHB, Thompson L, Anderson RA. Long term follow-up of survivors of childhood cancer: summary of updated SIGN guidance. BMJ 2013;346:f1190 doi: 10.1136/bmj.f1190
- Loren AW, Mangu PB, Beck LN, y col. Fertility preservation for patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol 2013;31(19):2500e10.
- Klipstein S, Fallat ME, Savelli S. Fertility preservation for pediatric and adolescent patients with cancer: medical and ethical considerations. Pediatrics 2020;145
- Anderson R.A, Mitchell RT, Thomas WK, y col. Cancer treatment and gonadal function: experimental and established strategies for fertility preservation in children and young adults. The Lancet. 2015, Vol 3. Issue 7: 556-567. doi.org/10.1016/S2213-8587(15)00039-X
- A.N Schuring. T.Fehm. K. Behrinher. M. y col. Practical recommendations for fertility preservation in women by the Ferti PROTEKT network. Part I: Indications for fertility preservation. Archives of Gynecology and Obstetrics .2018. Guidelines and position statements. https//dol.org/10.1007/s00404-017-4594-3
- Guzy, L; Demeestere, I.Assessment of ovarian reserve and fertility preservation strategies in children treated for cancer. Minerva Ginecológica, 2017, Feb; 69(1):57- 67
- Bisharah M, Tulandi T. Laparoscopic preservation of ovarian function: an underused procedure. Am J Obstet Gynecol. 2003 Feb;188(2):367-70. doi: 10.1067/mob.2003.38.
- Donnez J, Dolmans MM, Demylle D, y col.Live-birth after orthotopic transplantation of cryopreserved ovarian tissue. Lancet. 2004;364:1405–1410. doi:10.1016/S0140-6736(04)17222-X.
- Mulder, R, Fertility preservation for female patients with childhood, adolescent, and young adult cancer: recommendations from the PanCareLIFE Consortium and the International Late Effects of Childhood Cancer Guideline Harmonization Group.2021. Thelancet.com/oncology, Vol 22 February 2021
- Terenziani M,, Piva L, Meazza C, y col. Oophoropexy: a relevant role in preservation of ovarian function after pelvic irradiation. Fertil Steril 009.2018. Mar;91(3):935.e15-6. doi: 10.1016/j.fertnstert.2008.09.029.
- Oktay, Brittany E. Harvey, Ann H. Partridge, y col. Fertility Preservation in Patients With Cancer: ASCO Clinical Practice Guideline Update. 2018. Journal of Clinical Oncology 2018 36:19, 1994-2001
1. Fellow Ginecología Infanto Juvenil, Ginecología, Hospital Italiano de Buenos Aires Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
2. Fellow Cirugía pediátrica Oncológica, Hospital Italiano, Buenos Aires
3. Residente Cirugía Pediátrica, Hospital Italiano, Buenos Aires
4. Jefe de Sección Cirugía Pediátrica y Oncocirugía Pediátrica, Hospital Italiano de Buenos Aires
5. Jefa de Oncología Pediátrica, Pediatría, Hospital Italiano de Buenos Aires
6. Jefa Sección Fertilidad, Ginecología, Hospital Italiano de Buenos Aires.
7. Jefa Sección Ginecología Infanto Juvenil, Ginecología, Hospital Italiano de Buenos Aires.
8. Medica Planta de Ginecología, Sección Infanto Juvenil, Hospital Italiano de Buenos Aires.
9. Jefe de Servicio Cirugía Pediátrica. Hospital Italiano de Buenos Aires
10. Médica de Planta Cirugía Pediátrica, Sección Urología Pediátrica Hospital Italiano de Buenos Aires. Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
Hospital Italiano de Buenos Aires, Argentina.
Tte. Gral. Juan Domingo Perón 4190 – CABA

