Vacunación contra VPH en niñas y adolescentes
VPH Vaccination in children and adolescents
Artículo de Revisión
Dr. Silvio Tatti1, Dra. Agustina Puñal2, Dra. Laura Fleider3
Resumen
El 70% de la población adolescente se infectará por VPH. El conocimiento del VPH y sus distintos genotipos como agente causal del cáncer cervical nos permitió avanzar en la prevención primaria del mismo con la implementación de vacunas profilácticas. Estas están diseñadas para prevenir los cánceres producidos por el VPH y sus lesiones asociadas, dentro de las cuales cobra real importancia las verrugas genitales, altamente frecuentes en población adolescente.
En Argentina tenemos disponible la vacuna cuadrivalente que protege contra los tipos 6, 11, 16 y 18.
En el camino hacia la eliminación del cáncer cervical, el objetivo es que el 90% de las niñas menores de 15 años completen el esquema de vacunación.
Las tasas de vacunación aún no son óptimas, por lo tanto, debemos trabajar en estrategias orientadas al personal de salud y comunidad para lograr el objetivo.
Palabras clave: Virus del Papiloma Humano (VPH), Cáncer de cuello uterino, adolescentes, vacunación, vacuna cuadrivalente.
Abstract
70% of the adolescent population will be infected with HPV. Knowledge of HPV and its different genotypes as the causal agent of cervical cancer allowed us to advance in its primary prevention with the implementation of prophylactic vaccines. These are designed to prevent cancers caused by HPV and its associated lesions, among which genital warts, highly frequent in the adolescent population, take on real importance.
In Argentina we have available the quadrivalent vaccine that protects against types 6, 11, 16 and 18.
On the road to eliminating cervical cancer, the goal is for 90% of girls under 15 years of age to complete the vaccination schedule.
Vaccination rates are not yet optimal; therefore we must work on strategies aimed at health personnel and the community to achieve the goal.
Key words: HPV Vaccines – Cervical Cancer Prevention – intraepithelial lesions - adolescents
Introducción
Se considera al cáncer de cuello uterino (CCU) como uno de los mayores problemas de la Salud Pública a nivel mundial, muy especialmente en los países en vías de desarrollo, en los que sucede más del 80% de los casos; correspondiendo a aproximadamente el 10% de todos los cánceres detectados en mujeres1
A partir de la década del ´70, basados en los trabajos de Harald zur Hausen, se llegó a una definición en la etiología de la enfermedad al conocerse al virus del Papiloma Humano (VPH) y su relación directa con el CCU; detectándose la presencia de este en el 99.7% de estos cánceres, predominando los tipos de alto riesgo oncogénico, principalmente 16 y 18 (factor etiológico del 70% de ellos), seguidos en menor proporción por el 31 y 452,3
Aproximadamente el 70% de la población adolescente se infectará por VPH; la duración media de la infección será de seis a doce meses aproximadamente, pudiendo ser de mayor tiempo cuando los tipos involucrados son 16 y 184-5 El 10 al 20% de las mujeres infectadas, presentan persistencia viral y constituyen un grupo de riesgo para desarrollar cáncer cervical6
Gracias al conocimiento del VPH como agente causal del cáncer cervical se puede avanzar en la prevención de este, al neutralizar dicho agente mediante la administración de vacunas profilácticas.
Las vacunas contra el VPH están diseñadas para prevenir los cánceres producidos por el VPH y sus lesiones asociadas7-8, como las verrugas genitales, el cáncer y las lesiones pre-neoplásicas de cuello uterino, vulva, ano, vagina y pene; el cáncer de orofaringe y la papilomatosis respiratoria recurrente9-10
Vacunas contra el VPH
En Argentina tenemos disponible la vacuna cuadrivalente que protege contra los tipos 6, 11, 16 y 18.
No tienen capacidad infectante, debido a que las proteínas L1 se autoensamblan dando lugar a cápsides virales vacías morfológicamente idénticas al VPH 11-12-13-14; por lo que el organismo produce anticuerpos tipo específicos, diseñados especialmente para cada tipo de VPH.
Figura 1: Como se producen las vacunas contra el HPV15 Tomado de: https://slideplayer.com/slide/3348669/ acceso 27/3/202
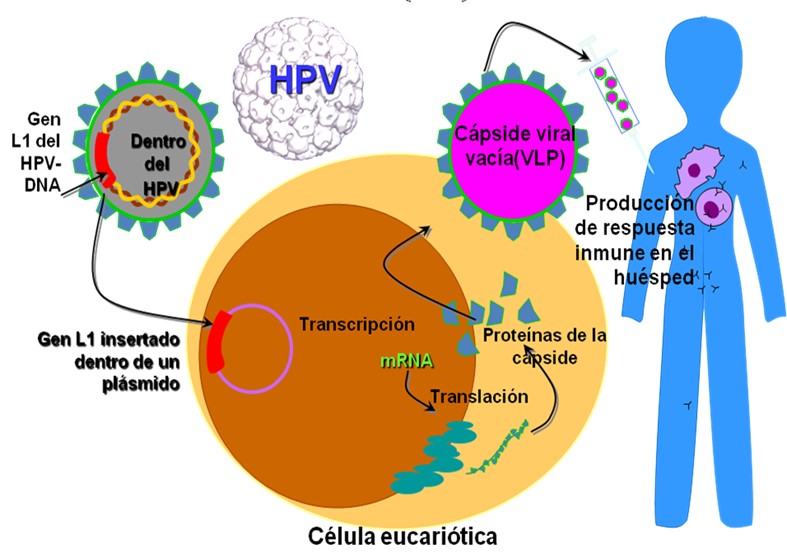
La respuesta inmune a la infección natural por VPH es lenta y débil, motivo por el cual sólo un 60% aproximadamente de los individuos infectados desarrollan anticuerpos contra el VPH16-17-18-19 De todas formas la infección por VPH es muy común y generalmente la mayoría de las lesiones regresa espontáneamente gracias a la inmunidad celular20
En contraste los anticuerpos otorgados por las vacunas son altos y se mantienen persistentes y en valores suficientes para otorgar protección, demostrada por ahora durante nueve años; que es el tiempo que dura el seguimiento de los trabajos de investigación, sin perder eficacia clínica con ninguna de ambas vacunas disponibles21 con una eficacia excelente 22-23 , ya que son administradas en forma intramuscular, por lo cual entran rápidamente a la sangre y se ponen en contacto con el sistema inmune y tienen adyuvantes24-25 y otorgan memoria inmune y protección cruzada26, todo esto demostrado en gran cantidad de ensayos clinicos27-28-29-30-31-32-33-34-35-36-37-38-39-40-41-42-43.
Cabe mencionar que la vacuna de la cual disponemos en el Calendario Nacional de Vacunación protege contra las verrugas genitales, patología muy frecuente en niñas y adolescentes, que se adquiere fácilmente luego del contacto con una pareja infectada44-45-46-47-48-49-50. En Australia se implementó el uso de la vacuna cuadrivalente en el Programa Nacional de Vacunación en el año 2007. Allí se realizó un estudio retrospectivo entre los años 2004 y 2011 en 36,055 pacientes51 en el cual se evaluó la incidencia de verrugas genitales luego de implementada la vacunación en mujeres. Comparando dos períodos de doce meses (2007-2008 versus 2010-2011), las verrugas genitales disminuyeron en mujeres menores de 21 años de 18.6% a 1.9% y en hombres heterosexuales menores de veintiún años de 22.9% a 2.9%. No se observó disminución de las verrugas genitales entre los hombres que mantienen sexo con hombres (Figura 2), lo que lleva a que actualmente en Australia se incluya a los niños de doce y trece años dentro del Plan Nacional de Vacunación, a partir del mes de febrero de 2013.
Figura 2: Disminución de verrugas genitales en Australia (Tomado de: The near disappearance of genital warts in young women 4 years after commencing a national human papillomavirus (HPV) vaccination programme Read T ,Hocking J y col Sex Transm Infect 2011;87:544e547. doi:10.1136/sextrans-2011-050234)
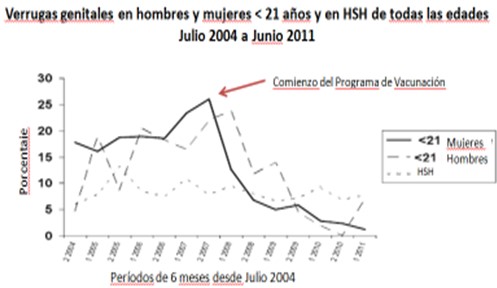
El hombre también se beneficia con la vacuna contra el VPH34-35-36-37.
La vacuna contra el VPH está aprobada para prevenir cáncer de cuello uterino, vagina, vulva y ano y verrugas genitales; siendo la última aprobación la prevención de la neoplasia intraepitelial anal52-53.
No debe aplicarse a mujeres embarazadas54-55 y se ha demostrado eficacia clínica en la población inmunocomprometida55-56
Esquemas de vacunación y duración de la eficacia
Los trabajos de investigación se realizaron con esquema de tres dosis dentro del año a toda edad57-58. Estudios posteriores demostraron que el nivel de anticuerpos en niñas y niños inmunocompetentes menores de 14 años es suficiente para tener un alto nivel de eficacia59-60, siendo actualmente la indicación en esquema de 2 dosis (0 - 6 meses) en individuos inmunocompetentes menores de 14 años; los mismos esquemas de vacunación rigen para la vacuna nonavalente, la cual ya se encuentra aprobada, pero no disponible en Argentina.
Situación actual de vacunación en el Mundo
Según estimaciones de la OMS y Unicef el 55% de los estados miembros han introducido la vacuna en Programas Nacionales de forma parcial o total. Para Globocan 2019 los países que han introducido la vacuna representan un 39% de la carga global de cáncer cervical.
Estamos en el camino hacia la eliminación del cáncer cervical, para ello el 90% de las mujeres tienen que estar vacunadas antes de los 15 años, el 70% de las mujeres testeadas para HPV entre los 35 y 45 años y el 90% de las mujeres con resultados positivos deben recibir tratamiento adecuado61
En la pandemia Covid 19 las tasas de vacunación en las niñas han disminuido y los esquemas han sido interrumpidos. Si se interrumpe el calendario de vacunación, no es necesario reiniciar el esquema. El número de dosis recomendadas se basa en la edad en el momento de la administración de la primera dosis.
Para que esto no ocurra es fundamental realizar a nuestras pacientes y sus padres o tutores consejería acerca de la vacunación contra el VPH siguiendo 5 escalones en la comunicación: enseñar, informar, comunicar, recomendar y vacunar.
Mejorando la vacunación contra el HPV en niñas y adolescentes
- Se debe considerar bajar la edad de vacunación entre las niñas de 11 años a las niñas de 9 años en quienes la vacuna está autorizada
- Menor edad de vacunación implica mejor adherencia, es decir mayor cantidad de niñas vacunadas.
- Nos garantizamos un bajo porcentaje de niñas que hayan iniciado las relaciones sexuales
- En Estados Unidos:
- El rango de vacunación a los 13 años fue del 68.1% vs el 51.1% a los 17 años
- El 40% de las adolescentes menores de 13 años completaron el esquema de vacunación
Para mejorar la cobertura debemos realizar las siguientes acciones:
- Entrenamiento a distancia de los efectores de los centros de vacunación
- Lecciones aprendidas de la pandemia COVID-19 en cuanto al registro informático de adolescentes vacunados evaluando sus debilidades
- Desarrollo de un Programa de educación para el HPV que incluya a la comunidad sobre todo en las poblaciones socialmente vulnerables. Estos Programas podrían estar basados en actividades ministeriales o ligados a la acción de las Universidades de cada Provincia, incluyendo el personal médico y paramédico
- La educación de los padres en la visita al pediatra y ginecólogo infanto-juvenil juega un rol central en la aceptación de esta vacuna; debe quitarse el estigma de ser una vacuna que incentiva la actividad sexual. Ya que protege contra el cáncer de cuello uterino, vagina, vulva, ano, pene y orofaríngeo. Es una vacuna neutra de género.
- En 2018 la vacuna contra el HPV tenía una cobertura promedio de 68% en las mujeres de 13 a 17 años.
- En 2018 la vacuna contra tétanos y difteria tenía una cobertura del 89% en la misma edad.
- La falta de recomendación de pediatras y/o ginecólogos infanto-juveniles fue la primera barrera para que esta vacuna no tenga una cobertura similar a las otras
- Los pediatras habitualmente piensan bajo evidencia que siempre volverán a ver a la niña de 9 años en sucesivos controles y postergan la indicación de la vacuna de HPV; es bien claro que a partir de los 11 años está incluida en el Programa nacional de Inmunizaciones la NO recomendación es una OPORTUNIDAD PERDIDA, ya que a medida que crece la niña se hace más difícil que ella o sus padres comprendan la necesidad de vacunarse
Conclusiones
La vacuna contra el VPH es una vacuna segura, que otorga alto título de anticuerpos, ha sido incluida en el Calendario Nacional de Vacunación en la Argentina para niñas y niños. Las tasas de vacunación aún no son óptimas y han disminuido durante la pandemia Covid 19. Es necesario que los médicos, especialmente los orientados en la atención de niñas, niños y adolescentes pensemos que los adolescentes se van a amoldar en el 2021 al pensamiento hegemónico de guías y programas. Los médicos vinculados a la temática debemos tener una visión constructivista de la dinámica de salud, lo que incluye que para lograr nuestros objetivos vacunales en la prevención del cáncer de cuello de útero deberíamos utilizar los recursos informáticos disponibles como mensajes de texto, YouTube, Facebook, Instagram y Twitter a través de las vías institucionales a las que pertenecemos.
Con información que incluya videos cortos, fotografías, historias personalizadas que motiven a los adolescentes a que pidan ser vacunados. Esto es crear la adherencia vacunal en nuestras pacientes adolescentes para que la repliquen en su comunidad y contactos.
Referencias
- Parkin DM. Cancer burden in the year 2000. The global picture. Eur J Ca 2001; 37:4-66
- Bosch FX, Lorincz A, Muñoz N, et al. The causal relation between Human Papillomavirus and Cervical Cancer J Clin Pathol 2002; 55:244-65
- Walboomers JM, Jacobs MV, Manos MM, et al. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J Pathol 1999; 189:12-19
- Ho GY, Bierman R ,Beardsley L, Chang CJ, Burk RD, et al. Natural History of Cervicovaginal Papillomavirus Infection in Young Women N Engl J Med 1998; 388: 423-28
- Depuydt CE, Vereachen AJ Salembier GM, et al. Thin-layer liquid-based cervical cytology and PCR for detecting and typing Human Papillomavirus DNA in Flemish Women Br J Cancer 2003; 88:560-66
- Schiffman M, Castle PE. Human Papillomavirus Epidemiology and Public Health Arch Pathol Lab Med 2003; 127:930-34
- Baden LR, Curfman GD, Morrissey S, Drazen JM. Human papillomavirus vaccine—opportunity and challenge. N Engl J Med 2007; 356:1990–91.
- Schiffman M, Wacholder S. From India to the world—a better way to prevent cervical cancer. N Engl J Med 2009; 360:1453–55
- World Health Organization. WHO/ICO Information Centre on Human Papilloma Virus (HPV) and Cervical Cancer. 2010 Summary Report. www.who.int/hpvcentreAcceso Octubre 2013
- Chaturvedi AK, Engels EA, Pfeiffer RM, et al. Human papillomavirus and rising oropharyngeal cancer incidence in the United States. J Clin Oncol 2011; 29:4294–301.
- Zhou J, Sun XY, Stenzel DJ, Frazer IH. Expression of vaccinia recombinant HPV 16 L1 and L2 ORF proteins in epithelial cells is sufficient for assembly of HPV virion-like particles. Virology 1991; 185:251–57.
- Kirnbauer R, Booy F, Cheng N, Lowy DR, Schiller JT. Papillomavirus L1 major capsid protein self-assembles into virus-like particles that are highly immunogenic. Proc Natl Acad Sci USA 1992; 89:12180– 84.
- Schiller JT, Lowy DR. Papillomavirus-like particles and HPV vaccine development. Semin Cancer Biol 1996; 7:373–82.
- Harro CD, Pang YY, Roden RB, et al. Safety and immunogenicity trial in adult volunteers of a human papillomavirus 16 L1 virus-like particle vaccine. J Natl Cancer Inst 2001; 93:284–92.
- http://www.womeningovernment.org/home/koutsky acceso 23/4/2008 https://slideplayer.com/slide/3348669/ acceso 27/3/2022
- Geijersstam V, Kibur M, Wang Z, et al. Stability over time of serum antibody levels to human papillomavirus type 16. J Infect Dis 1998; 177:1710–14.
- Safaeian M, Porras C, Schiffman M, et al; Costa Rican Vaccine Trial Group. Epidemiological study of anti-HPV16/18 seropositivity and subsequent risk of HPV16 and -18 infections. J Natl Cancer Inst 2010; 102:1653–62.
- Tindle RW. Immune evasion in human papillomavirus-associated cervical cancer. Nat Rev Cancer 2002; 2:59–65.
- Scott M, Nakagawa M, Moscicki AB. Cell-mediated immune response to human papillomavirus infection. Clin Diagn Lab Immunol 2001; 8:209–20.
- Wang SS, Hildesheim A. Chapter 5: Viral and host factors in human papillomavirus persistence and progression. J Natl Cancer Inst Monogr 2003; 31:35–40.
- De Carvalho N, Teixeira J, Roteli-Martins CM, et al. Sustained efficacy and immunogenicity of the HPV-16/18 AS04-adjuvanted vaccine up to 7.3 years in young adult women. Vaccine 2010; 28:6247–55.
- Smith JF, Brownlow M, Brown M, et al. Antibodies from women immunized with Gardasil cross-neutralize HPV 45 pseudovirions. Hum Vaccin 2007; 3:109–15.
- Rowhani-Rahbar A, Mao C, Hughes JP, et al. Longer term efficacy of a prophylactic monovalent human papillomavirus type 16 vaccine. Vaccine 2009; 27:5612–19.
- Stanley M. HPV - immune response to infection and vaccination. Infect Agent Cancer 2010; 5:19.
- Stanley M. Pathology and epidemiology of HPV infection in females. Gynecol Oncol 2010; 117:5–10.
- Roberts JN, Buck CB, Thompson CD, et al. Genital transmission of HPV in a mouse model is potentiated by nonoxynol-9 and inhibited by carrageenan. Nat Med 2007; 13:857–61.
- Koutsky LA, Ault KA, Wheeler CM, et al. A controlled trial of a human papillomavirus type 16 vaccine. N Engl J Med 2002; 347:1645-47.
- Harper DM, Franco EL Wheeler C, et al. Efficacy of a bivalent L1 virus like-particle vaccine in prevention of infection with human papillomavirus 16 and 18 in young women: a randomized controlled trial. Lancet 2004; 364:1757-64.
- Villa LL, Costa RL, Petta CA, et al. Prophylactic quadrivalent human papillomavirus (types 6, 11, 16 y 18) L1 virus like particles vaccine in young women: a randomised double-blind placebo controlled phase II efficacy trial. Lancet Oncol 2005; 6:271-78.
- Garland S, Hernandez -Avila M, Wheeler CM, et al. Quadrivalent Vaccine against human papillomavirus to prevent anogenital disease. N Engl J Med 2007; 356:1928-43
- FUTURE II Study Group.Quadrivalent Vaccine against Human Papillomavirus to Prevent High-Grade Cervical Lesions N Engl J Med 2007; 356: 1915-27.
- Joura EA, Garland SM, Paavonen J, et al. Effect of the human papillomavirus (HPV) quadrivalent vaccine in a subgroup of women with cervical and vulvar disease: retrospective pooled analysis of trial data. BMJ 2012; 344: e140 doi: 10.1136/bmj.e1401 (Published 27 March 2012)
- Paavonen J, Naud P, Salmerón J, et al.HPV PATRICIA Study Group. Efficacy of human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine against cervical infection and precancer caused by oncogenic HPV types (PATRICIA): final analysis of a double-blind, randomized study in young women. Lancet 2009; 374:301–14.
- Giuliano AR, Palefsky JM, Goldstone S, et al. Efficacy of quadrivalent HPV vaccine against HPV Infection and disease in males. N Engl J Med 2011; 364:401–11.
- Palefsky JM, Giuliano AR, Goldstone S, et al. HPV vaccine against anal HPV infection and anal intraepithelial neoplasia. N Engl J Med 2011; 365:1576–85.
- Petäjä T, Keränen H, Karppa T, et al. Immunogenicity and safety of human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine in healthy boys aged 10-18 years. J Adolesc Health 2009; 44: 33–40.
- Reisinger KS, Block SL, Lazcano-Ponce E, et al. Safety and persistent immunogenicity of a quadrivalent human papillomavirus types 6, 11, 16, 18 L1 virus-like particle vaccine in preadolescents and adolescents: a randomized controlled trial. Pediatr Infect Dis J 2007; 26:201–09.
- Muñoz N, Manalastas Jr R, Pitisuttithum P, et al. Safety, immunogenicity, and efficacy of quadrivalent human papillomavirus (types 6, 11, 16, 18) recombinant vaccine in women aged 24-45 years: a randomised, double-blind trial. Lancet 2009; 373:1949–57
- Castellsague X., Muñoz N., Pitisuttithum P, et al. End-of-study safety, immunogenicity, and efficacy of quadrivalent HPV (types 6, 11, 16, 18) recombinant vaccine in adult women 24–45 years of age BJC 2011; 105:28-37
- Schwarz TF, Spaczynski M, Schneider A, et al. Immunogenicity and tolerability of an HPV-16/18 AS04-adjuvanted prophylactic cervical cancer vaccine in women aged 15-55 years. Vaccine 2009; 27: 581–87.
- Malagon T., Drolet M, Boily MC,et al. Cross-Protective efficacy of two human papillomavirus vaccines: a systematic review and meta-analysis The Lancet Inf Dis 2012 Accesado el 1 de septiembre de 2012 en http://dx.doi.org/10.1016/S1473-3099(12)70187-1
- Brown DR, Kjaer SK, Sigurdsson K, et al. The impact of quadrivalent human papillomavirus (HPV; types 6, 11, 16, and 18) L1 virus-like particle vaccine on infection and disease due to oncogenic nonvaccine HPV types in generally HPV-naive women aged 16-26 years. J Infect Dis 2009; 199 :926-35
- Wheeler C., Castellsagué X. , Garland S., et al. Cross-protective efficacy of HPV-16/18 AS04-adjuvanted vaccine against cervical infection and precancer caused by non-vaccine oncogenic HPV types: 4-year end-of-study analysis of the randomised, double-blind PATRICIA trial. Lancet Oncol 2012; 13:100-10
- Kjaer S., Tran T., Sparen P, et al. The Burden of Genital Warts: A Study of Nearly 70,000 Women from the General Female Population in the 4 Nordic Countries JID 2007; 196:1447-54
- Insinga RP, Dasbach EJ., Myers El. The health and economic burden of genital warts in a set of private health plans in the United States. Clin Infect Dis 2003; 36:1397-403
- http://www.hpa.org.uk/cdr/archives/2001/cdr3501.pdf
- Koutsky L. Epidemiology of genital human papillomavirus infection Am J Med 1997; 102:3–8
- Cuschieri KS, Cubie HA, Whitley MW, et al. Multiple high risk HPV infections are common in cervical neoplasia and young women in a cervical screening population. J Clin Pathol. 2004; 57: 68-72
- http://www.cdc.gov/std/hpv/common-linicians/sp/ClinicianBro-Sp-fp.pdf
- Palefsky JM. Human Papillomavirus-related disease in people with HIV. Curr Opin HIV AIDS 2009; 4:52–56
- Read T., Hocking J., Chen MY., Donovan B., Bradshaw CS., Fairley CK. The near disappearance of genital warts in young women 4 years after commencing a national human papillomavirus (HPV) vaccination programme Sex Transm Infect 2011; 87:544-47
- Center for Disease Control and Prevention (CDC) FDA Licensure of Quadrivalent Human Papillomavirus Vaccine (HPV4, Gardasil) for Use in Males and Guidance from the Advisory Committee on Immunization Practices (ACIP) MMWR 2010; 59:630-32
- http://www.anmat.gov.ar/boletin_anmat/septiembre_2012/Dispo_5598-12.pdf
- Centers for Disease Control and Prevention (CDC). FDA licensure of bivalent human papillomavirus vaccine (HPV2, Cervarix) for use in females and updated HPV vaccination recommendations from the Advisory Committee on Immunization Practices (ACIP). MMWR 2010; 59:626-29
- Markowitz L., Dunne E., Saraiya M., et al. Quadrivalent Human Papillomavirus Vaccine Recommendations of the Advisory Committee on Immunization Practices (ACIP) MMWR 2007; 56:1-24 http://www.cdc.gov/mmwr/preview/mmwrhtml/rr5602a1.htm
- Advisory Committee on Immunization Practices. Recommended adult immunization schedule: United States, 2010. Ann Intern Med 2010; 152:36-39
- Roteli-Martins C., Naud P., De Borba P.,et al. Sustained immunogenicity and efficacy of the HPV-16/18 AS04-adjuvanted vaccine Up to 8.4 years of follow-up Hum Vaccin Immunother 2012; 390-97
- S. K. Kjaer. Nordic Long Term Follow-up of Effectiveness, Immunogenicity, and Safety of Gardasil™. 27th International Papillomavirus Conference and Clinical Workshop. Berlín. Germany. September 17-22, 2011 P.01.36
- Romanowski B., Schwartz T., Ferguson LM., et al. Immunogenicity and safety of the HPV-16/18 AS04-adjuvanted vaccine administered as a 2-dose schedule compared with the licensed 3-dose schedule: results from a randomized study. Human Vaccines 2011; 7:1374-86
- Neuzil K., Canh Do G., Thiem VD., et al. Immunogenicity and Reactogenicity of Alternative Schedules of HPV Vaccine in Vietnam A Cluster Randomized Noninferiority Trial JAMA 2011; 305:1424-31
- OMS. Global Strategy to accelerate the elimination of cervical cancer as a public health problem htpps://www.who.int/publications/i/item/9789240014107
¹ Prof. Titular de Ginecología de la UBA, Director del programa de Prevención, Diagnóstico, Terapéutica y Vacunación en Patologías del TGI del Hospital de Clínicas “José de San Martín” UBA, Director de la Carrera de Médico especialista en Patologías del Tracto Genital Inferior de la Universidad de Buenos Aires
² Médica ginecóloga del programa de Prevención, diagnóstico, terapéutica y vacunación en el TGI. Division Ginecologia Hospital de Clinicas “Jose de San martin” UBA
³ Doc. Aut. Ginecología UBA, Jefa Sección Patología Cervical del Hospital de Clínicas “José de San Martín” UBA, Subdirectora de la Carrera de Médico Especialista en Patologías del Tracto Genital Inferior de la Universidad de Buenos Aires
División Ginecología Hospital de Clínicas “José de San Martín” UBA
Córdoba 2351, C1028 CABA Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
.

